(通讯员:王珂)近日,我校动物科学技术学院、动物医学院崔旻教授团队与英国卡迪夫大学杨欣副教授团队研发了一种利用声镊操控技术——声表面波(surface acoustic wave,SAW)改变血脑屏障(blood-brain barrier,BBB)通透性的方法。相关成果以Open source board based acoustofluidic transwells for reversible disruption of the blood–brain barrier for therapeutic delivery为题,发表在Biomaterials Research上。这项技术可在不改变BBB的结构情况下精准的调控BBB的打开/关闭,有望实现中枢神经系统(central nervous system,CNS)可控的药物递送。
随着神经退行性疾病(如阿尔兹海默症和帕金森综合症等)和CNS感染性疾病受到越来越多的关注,如何高效安全地实现CNS的药物递送当前仍是一个巨大的挑战。传统的CNS药物递送方法均有一定的局限性,开发新型的CNS药物递送方案迫在眉睫。
SAW是一种沿着介质表面传播的声波,基于能量集中和易于操控等特性,近年来SAW应用于生物医学领域,包括细胞筛选、细胞特性研究和细胞分化等方面。
为了探究SAW是否可用于BBB的调控,研究团队合作开发了一种柔性印刷电路板的声流体生物反应器(PCB-AFB),用于BBB体外模型及斑马鱼模型的研究。利用欧姆计测定BBB体外模型的跨内皮电阻,及对各类分子的细胞旁通透性,分析BBB的功能。
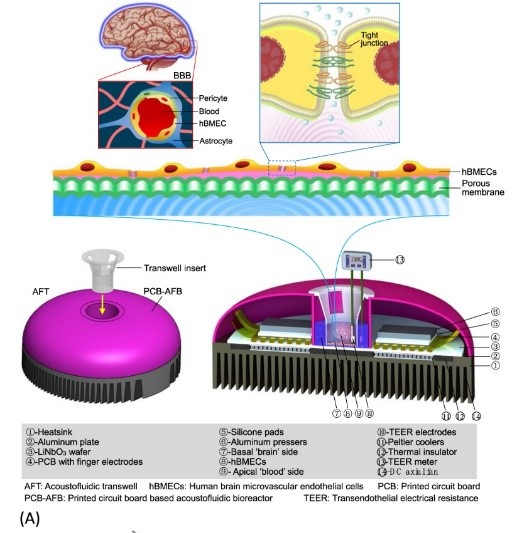
声流体生物反应器(PCB-AFB)模式图(左)和SAW作用于人脑微血管内皮细胞打开细胞间隙(右)
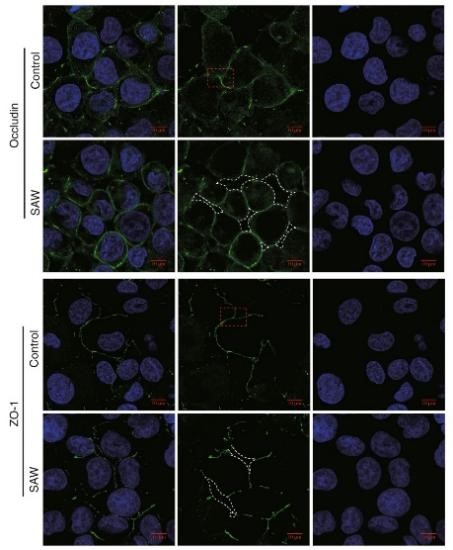
研究发现PCB-AFB通过声辐射和声流体作用于BBB。SAW在一定程度上呈现作用时间和作用功率的依赖性。SAW的刺激几乎不影响人脑微血管内皮细胞的细胞活性,不改变紧密连接蛋白的表达,但改变了邻近细胞紧密连接蛋白的分布,扩大内皮细胞的细胞间隙,从而增加了BBB对小分子物质(NaF,376 dalton)和大分子物质(FITC-Dextran-10 kD,FITC-Dextran-70 kD)的通透性。SAW刺激BBB后,经过一段时间BBB功能可以自行恢复。该研究提示,通过控制SAW的作用功率,可以实现可逆地开关BBB,实施CNS药物的精准递送。
我校动物科学技术学院、动物医学院博士后王珂与西北工业大学助理教授孙超为该论文的共同第一作者;我校动物科学技术学院、动物医学院崔旻教授与英国卡迪夫大学杨欣副教授为论文的共同通讯作者,此外大连理工大学、浙江大学、英国诺森比亚大学和华中科技大学同济医学院等多家单位共同参与了此项研究。该研究得到了国家重点研发计划项目、自然科学基金、英国工程与自然科学研究委员会基金和国际交流基金的资助。
全文链接:https://doi.org/10.1186/s40824-023-00406-6
审核人:崔旻

